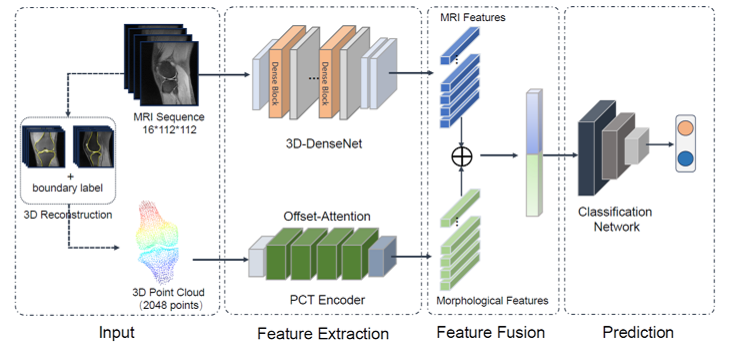
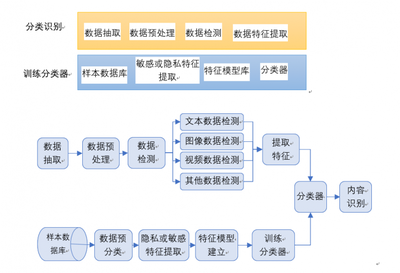
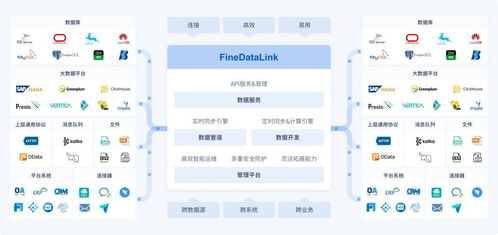
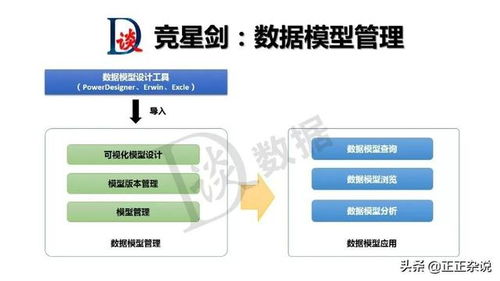
生物医学影像,如CT、MRI、PET、超声及各类显微镜成像,是现代医学诊断、治疗规划和基础研究的基石。原始影像数据本身蕴含的信息往往被噪声、伪影及复杂背景所掩盖。因此,数据处理技术成为将原始像素数据转化为可靠生物学信息与临床洞见的关键桥梁。这一系列技术贯穿于影像的获取、分析、解释与应用全链条,正日益成为推动精准医疗发展的核心引擎。
1. 数据预处理:影像质量的“净化器”
预处理是后续所有分析的基础,旨在提升影像质量与一致性。
- 降噪与增强:采用滤波技术(如高斯滤波、中值滤波、非局部均值滤波)抑制随机噪声,同时通过直方图均衡化、对比度拉伸等方法增强目标组织与背景的对比度。
- 图像配准:将不同时间点、不同模态(如MRI与PET)或不同个体获取的影像在空间上进行对齐。这对于疾病进展追踪、多模态信息融合至关重要,通常涉及刚性与非刚性变换算法。
- 不均匀性校正:尤其常见于MRI,用于纠正由射频场不均匀性导致的亮度变化,确保组织信号强度的真实性。
2. 图像分割:结构与区域的“识别者”
分割旨在将影像划分为具有不同解剖或病理意义的区域,是量化分析的前提。
- 传统方法:包括阈值法、区域生长、边缘检测以及基于图论的方法(如图割)。这些方法计算效率高,但常对噪声敏感,自动化程度有限。
- 机器学习与深度学习:当前的主流与前沿。从支持向量机、随机森林等传统机器学习,到以U-Net、V-Net及其众多变体为代表的卷积神经网络(CNN),深度学习能够自动学习层次化特征,在肿瘤、器官(如心脏、肝脏)、细胞核等复杂目标的精确分割上表现出色,大大减少了人工干预。
3. 特征提取与量化:信息的“翻译官”
分割后,需要从目标区域中提取定量特征,将视觉信息转化为可计算、可比较的数据。
- 形态学特征:如体积、表面积、周长、紧凑度等。
- 强度特征:如均值、方差、纹理特征(通过灰度共生矩阵等计算)。
- 高阶特征:在肿瘤影像组学中,可提取数百至上千个定量特征,描述肿瘤内部的异质性、空间模式等,为预后预测和治疗反应评估提供深层信息。
4. 数据管理与集成:多源信息的“枢纽站”
随着多模态成像、纵向研究和多中心协作的普及,高效的数据管理变得至关重要。
- 标准化格式:DICOM是医学影像存储与传输的全球标准,确保数据的互操作性。
- 数据库与PACS:影像归档与通信系统实现了影像的集中存储、检索和分发。
- 信息融合:将影像数据与患者的电子病历、基因组学、蛋白质组学等多组学数据整合,构建全面的患者数字画像,是实现真正个性化医疗的基础。
5. 分析与建模:洞见的“挖掘机”
这是从数据到知识的最后一步,旨在发现模式、建立预测模型。
- 统计分析:用于比较组间差异、识别相关性。
- 机器学习建模:利用提取的特征训练分类器(如区分良恶性肿瘤)或回归模型(如预测生存期)。深度学习中的端到端模型甚至可以直接从原始影像中学习并完成诊断分类任务。
- 可视化与解释:通过三维重建、体绘制等技术直观展示解剖结构与病变,并利用类激活图等可解释性AI技术理解模型的决策依据,增强临床信任。
挑战与未来展望
尽管技术飞速发展,挑战依然存在:数据标注成本高昂且需专业知识;模型的可解释性与泛化能力有待提升;数据隐私与安全法规严格。生物医学影像数据处理技术将朝着更自动化、更智能、更融合的方向演进。联邦学习可在保护隐私的前提下利用多中心数据训练更鲁棒的模型;生成式AI(如扩散模型)可用于数据增强和合成高质量影像;与手术机器人、放疗设备等的实时集成,将推动诊疗流程的闭环智能化。
总而言之,生物医学影像数据处理技术是一个快速迭代、深度交叉的领域。它不仅是图像处理算法在医学领域的应用,更是临床需求驱动下,融合了计算机科学、数学、物理学和生物医学知识的系统工程。其持续进步,正不断拓宽我们窥探生命奥秘、守护人类健康的视野与能力。